貝類過敏 DNA 疫苗免疫療法
Shellfish Allergy DNA Vaccine Immunotherapy
為何需要新的貝類過敏治療方向
貝類過敏是一種常見且可能嚴重的食物過敏,可引致皮膚、腸胃及呼吸道症狀,嚴重時甚至可出現過敏性休克 (Anaphylaxis)。目前臨床管理仍主要依賴避免接觸致敏原、飲食限制及意外暴露後的緊急處理,尚未有已廣泛應用、可直接改變過敏免疫反應的治療方案。
貝類過敏 DNA 疫苗免疫療法是一項面向未來的創新研發方向,聚焦於貝類主要致敏蛋白原肌球蛋白 (Tropomyosin, TM),並以低致敏性致敏原作為設計基礎,期望透過更精準的免疫調節,為貝類過敏帶來更安全及更具轉化潛力的新治療路向。現階段相關成果主要屬前臨床研究,並正持續推進至臨床轉化階段。

技術原理:低致敏性 DNA 疫苗如何重塑免疫反應
貝類過敏的主要致敏原之一是原肌球蛋白。研究團隊以低致敏性致敏原 MEM49 為基礎,透過基因工程降低其與免疫球蛋白 E (IgE) 的結合能力,同時保留可誘導免疫調節的關鍵表位。這個設計的目標,是讓免疫系統學習以較溫和的方式辨認致敏原,而不是觸發典型的過敏反應。
MEM49 的編碼序列被置入 DNA 疫苗載體後,會以較低風險的方式在體內提供抗原訊息,進一步誘導調節性 T 細胞 (Treg) 與抑制性抗體反應,推動免疫耐受的形成。與傳統過敏原特異性免疫治療 (Allergen-Specific Immunotherapy, ASIT) 逐步暴露的模式相比,DNA 疫苗策略希望以較少次數、較少劑量,達到更穩定的免疫重塑效果。
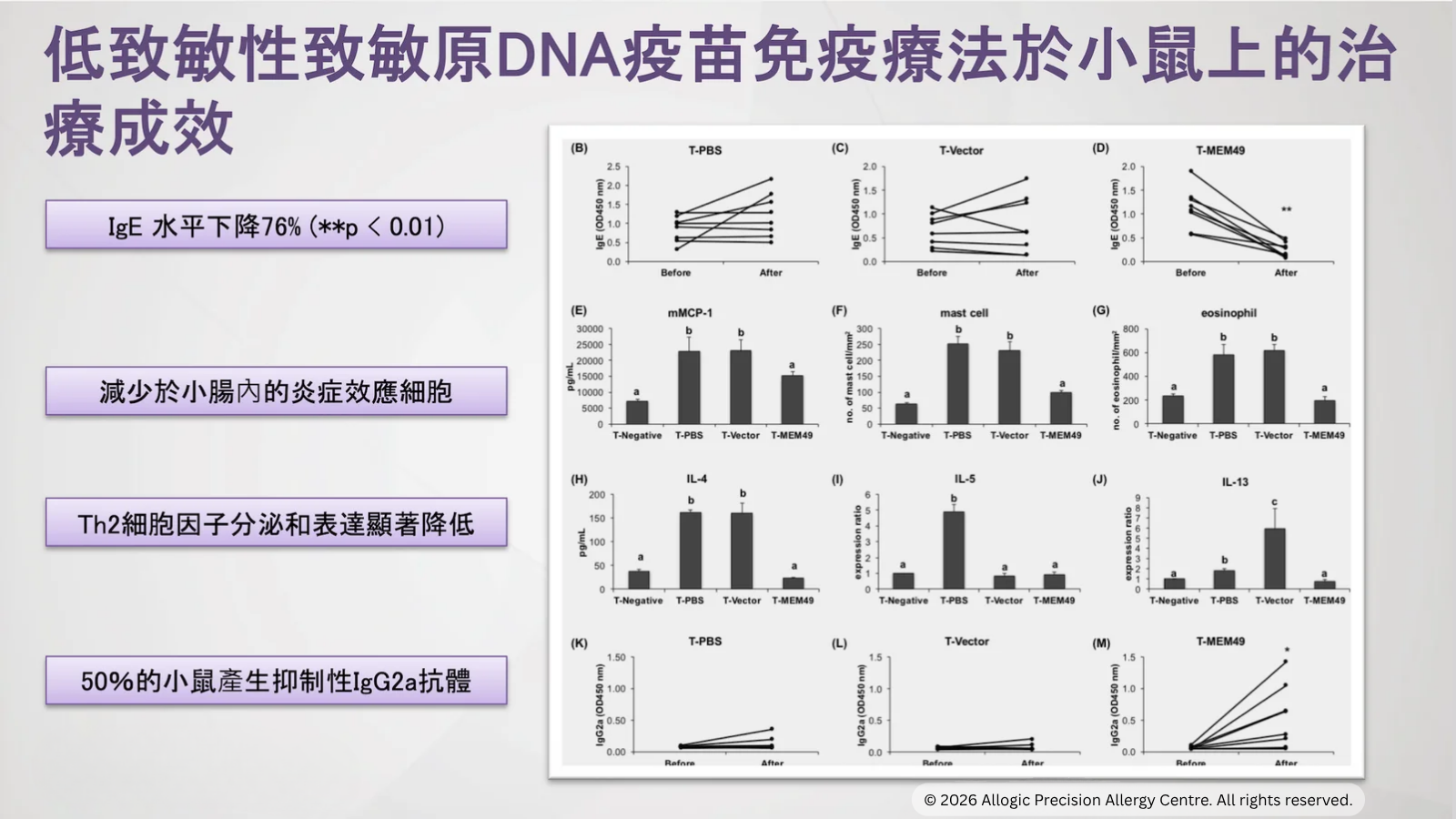
前臨床研究顯示,這項設計可顯著降低特異性 IgE 水平、抑制 Th2 型炎症反應,並減少過敏效應細胞活化,反映其具備降低過敏反應的潛力。現階段相關工作仍屬研發與轉化階段,重點在於進一步優化載體設計、安全性與臨床可行性。
研發進程:從前臨床到臨床轉化
前臨床結果顯示,低致敏性致敏原 MEM49 所設計的 DNA 疫苗具有免疫調節潛力,但要真正進入臨床應用,仍需完成載體優化、機制確認、安全性評估及人體研究設計等重要步驟。研究團隊目前正沿著這條轉化路線推進,目標是建立更穩定、可重複,並符合臨床標準的貝類過敏免疫療法。
這一階段的重點包括:透過表位改造建立 MEM49 設計、進行體外細胞分析以確認調節路徑、在動物模型中進一步評估安全性與療效,以及為後續人體研究作準備。這些步驟有助於把早期研究發現,逐步轉化為更可行的臨床方案。
展望未來,研究團隊計劃在更多機制與安全性數據支持下,繼續優化候選疫苗,並推進更接近臨床應用的研究設計。 若後續結果持續正面,這條路線有望為貝類過敏患者帶來一個更具針對性、且可能減少重複暴露風險的新選擇。

這項低致敏性致敏原 DNA 疫苗研發,旨在為貝類過敏提供更安全、更具轉化潛力的治療方向。

為未來治療帶來更多希望

連結機制研究與臨床轉化